“GST亲和层析介质”详细介绍
简介
GST亲和层析介质(GST Agarose)是专门设计用于纯化谷胱甘肽S-转移酶(GST)融合蛋白、其它谷胱甘肽转移酶以及与谷胱甘肽有亲和作用蛋白的分离介质,一步分离就可得到高纯度的GST融合目标蛋白,纯化条件温和,可以保证蛋白的活性。
本产品是自主设计合成的GST琼脂糖凝胶,具有优良的物理和化学稳定性,使用寿命长,操作方便,批次重复性好,易于放大,是研发与生产的理想选择。
适用范围
分离谷胱甘肽S-转移酶(GST)融合蛋白、其它谷胱甘肽转移酶以及与谷胱甘肽有亲和作用的蛋白。
玻璃层析柱
1)将层析柱洗净后垂直固定到铁架台上;向柱中加入蒸馏水,排开柱子中的空气,在蒸馏水排尽以前,关闭柱子出口,在柱内保留5~8cm高度的蒸馏水。
2)先将介质混匀,用移液枪按需要量吸取介质,或用玻璃棒紧靠柱子内壁引流,将介质加入到层析柱中;静置30min,让介质自然沉降。
3)从上端管口将转换杆出液端缓慢推至介质沉降平面,使介质表面保持水平状态,注意避免转换杆与介质接触面间滞留气泡。
4)在使用一段时间后,如果流速减慢,可先卸下上转换杆,将介质倒出,再取出下转换接头中滤网,清洗或更换后重新装柱。
4.过柱:
1)用10倍介质体积缓冲液A过柱,平衡介质;
2)上样;
3)用5~10倍介质体积缓冲液A过柱,洗去层析柱中剩余上样液并重新平衡介质;
4)用5~10倍介质体积缓冲液B洗脱,收集洗脱液;
5)用5~10倍介质体积缓冲液A重新平衡介质。
注:纯化过程流速不宜过快,对于1ml介质,流速保持在0.5ml/min为宜。
1)沉淀或变性物质的清洗:
用2倍介质体积6 M盐酸胍清洗,然后用5倍介质体积缓冲液A平衡介质。
2)疏水缔合物质的清洗:
用3~4倍介质体积70%乙醇(或2倍介质体积去垢剂,如 1%Triton?X-100)清洗介质;然后用5倍介质体积缓冲液A平衡介质。
介质保存
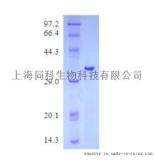
4℃~8℃条件下,介质可长期保存于20%乙醇中。1.低分子量Marker;2.上样液;3.GST-流穿液;4.GST-洗脱液;5.对照-流穿液;6.对照-洗脱液
GST亲和层析介质使用注意事项
1.GST融合蛋白与还原型谷胱甘肽的结合比较缓慢,为获得最大结合量,需要保证足够的作用时间,因而在上样时要维持较低流速。在样品中加入5~10mM DTT可以增加介质对目标蛋白的吸附。对于按常规步骤操作吸附效果不好的样品,可以先把介质和样品混合,轻轻振摇2~4h,再装柱,用平衡缓冲液进行重新平衡、洗脱等操作。
2.不同的GST融合蛋白取得最佳纯化效果所需还原型谷胱甘肽浓度、洗脱体积和洗脱时间可能有所不同。必要时需对流穿液、洗脱液进行SDS-PAGE以及Western杂交分析,以确定最佳纯化条件。
3.GST融合蛋白以包涵体形式存在时不能与介质结合,必须先进行变性、复性、透析处理后才能用介质进行纯化。纯化效果取决于复性效率。
4.纯化后出现杂带的常见原因
1)目标蛋白断裂或酶解
解决方案:向缓冲液A和缓冲液B中加入1mM PMSF抑制蛋白酶活性,或0.1%TritonX-100或0.1%Tween-20等稳定剂。
2)GST融合蛋白不完全表达
GST融合蛋白有时候只表达到GST部分就终止,GST标签蛋白连同完全表达的融合蛋白均能与介质结合并被洗脱下来,因而洗脱液中出现26KD左右的杂带。
解决方案:尝试用不同浓度的还原型谷胱甘肽洗脱;优化表达条件,降低GST融合蛋白不完全表达量;改变外源基因在载体中插入的酶切位点,重新构建表达载体;在不改变外源基因两端酶切位点的情况下,更换通用载体。
5.如后续实验需要除去洗脱液中还原型谷胱甘肽,可采用超滤或透析的方法。
GST标签可用位点专一的蛋白酶如凝血酶或Xa因子从融合蛋白中切除。蛋白酶解后,再用GST亲和层析方法去除GST标签,目标蛋白存在于流出液中。一般情况下,与切除GST标签后得到的外源蛋白相比,凝血酶用量极小,如果后续实验要求不严格,不需进一步除去与外源蛋白共存与洗脱液中的凝血酶。如需除去凝血酶,则可将样品用pH7~8的缓冲液溶解,然后直接过1ml的苯甲脒琼脂糖凝胶或者肝素琼脂糖凝胶吸附凝血酶。
GST亲和层析介质(GST Agarose)是专门设计用于纯化谷胱甘肽S-转移酶(GST)融合蛋白、其它谷胱甘肽转移酶以及与谷胱甘肽有亲和作用蛋白的分离介质,一步分离就可得到高纯度的GST融合目标蛋白,纯化条件温和,可以保证蛋白的活性。
本产品是自主设计合成的GST琼脂糖凝胶,具有优良的物理和化学稳定性,使用寿命长,操作方便,批次重复性好,易于放大,是研发与生产的理想选择。
适用范围
分离谷胱甘肽S-转移酶(GST)融合蛋白、其它谷胱甘肽转移酶以及与谷胱甘肽有亲和作用的蛋白。
玻璃层析柱
1)将层析柱洗净后垂直固定到铁架台上;向柱中加入蒸馏水,排开柱子中的空气,在蒸馏水排尽以前,关闭柱子出口,在柱内保留5~8cm高度的蒸馏水。
2)先将介质混匀,用移液枪按需要量吸取介质,或用玻璃棒紧靠柱子内壁引流,将介质加入到层析柱中;静置30min,让介质自然沉降。
3)从上端管口将转换杆出液端缓慢推至介质沉降平面,使介质表面保持水平状态,注意避免转换杆与介质接触面间滞留气泡。
4)在使用一段时间后,如果流速减慢,可先卸下上转换杆,将介质倒出,再取出下转换接头中滤网,清洗或更换后重新装柱。
4.过柱:
1)用10倍介质体积缓冲液A过柱,平衡介质;
2)上样;
3)用5~10倍介质体积缓冲液A过柱,洗去层析柱中剩余上样液并重新平衡介质;
4)用5~10倍介质体积缓冲液B洗脱,收集洗脱液;
5)用5~10倍介质体积缓冲液A重新平衡介质。
注:纯化过程流速不宜过快,对于1ml介质,流速保持在0.5ml/min为宜。
1)沉淀或变性物质的清洗:
用2倍介质体积6 M盐酸胍清洗,然后用5倍介质体积缓冲液A平衡介质。
2)疏水缔合物质的清洗:
用3~4倍介质体积70%乙醇(或2倍介质体积去垢剂,如 1%Triton?X-100)清洗介质;然后用5倍介质体积缓冲液A平衡介质。
介质保存
4℃~8℃条件下,介质可长期保存于20%乙醇中。1.低分子量Marker;2.上样液;3.GST-流穿液;4.GST-洗脱液;5.对照-流穿液;6.对照-洗脱液
GST亲和层析介质使用注意事项
1.GST融合蛋白与还原型谷胱甘肽的结合比较缓慢,为获得最大结合量,需要保证足够的作用时间,因而在上样时要维持较低流速。在样品中加入5~10mM DTT可以增加介质对目标蛋白的吸附。对于按常规步骤操作吸附效果不好的样品,可以先把介质和样品混合,轻轻振摇2~4h,再装柱,用平衡缓冲液进行重新平衡、洗脱等操作。
2.不同的GST融合蛋白取得最佳纯化效果所需还原型谷胱甘肽浓度、洗脱体积和洗脱时间可能有所不同。必要时需对流穿液、洗脱液进行SDS-PAGE以及Western杂交分析,以确定最佳纯化条件。
3.GST融合蛋白以包涵体形式存在时不能与介质结合,必须先进行变性、复性、透析处理后才能用介质进行纯化。纯化效果取决于复性效率。
4.纯化后出现杂带的常见原因
1)目标蛋白断裂或酶解
解决方案:向缓冲液A和缓冲液B中加入1mM PMSF抑制蛋白酶活性,或0.1%TritonX-100或0.1%Tween-20等稳定剂。
2)GST融合蛋白不完全表达
GST融合蛋白有时候只表达到GST部分就终止,GST标签蛋白连同完全表达的融合蛋白均能与介质结合并被洗脱下来,因而洗脱液中出现26KD左右的杂带。
解决方案:尝试用不同浓度的还原型谷胱甘肽洗脱;优化表达条件,降低GST融合蛋白不完全表达量;改变外源基因在载体中插入的酶切位点,重新构建表达载体;在不改变外源基因两端酶切位点的情况下,更换通用载体。
5.如后续实验需要除去洗脱液中还原型谷胱甘肽,可采用超滤或透析的方法。
GST标签可用位点专一的蛋白酶如凝血酶或Xa因子从融合蛋白中切除。蛋白酶解后,再用GST亲和层析方法去除GST标签,目标蛋白存在于流出液中。一般情况下,与切除GST标签后得到的外源蛋白相比,凝血酶用量极小,如果后续实验要求不严格,不需进一步除去与外源蛋白共存与洗脱液中的凝血酶。如需除去凝血酶,则可将样品用pH7~8的缓冲液溶解,然后直接过1ml的苯甲脒琼脂糖凝胶或者肝素琼脂糖凝胶吸附凝血酶。





 通过认证
通过认证